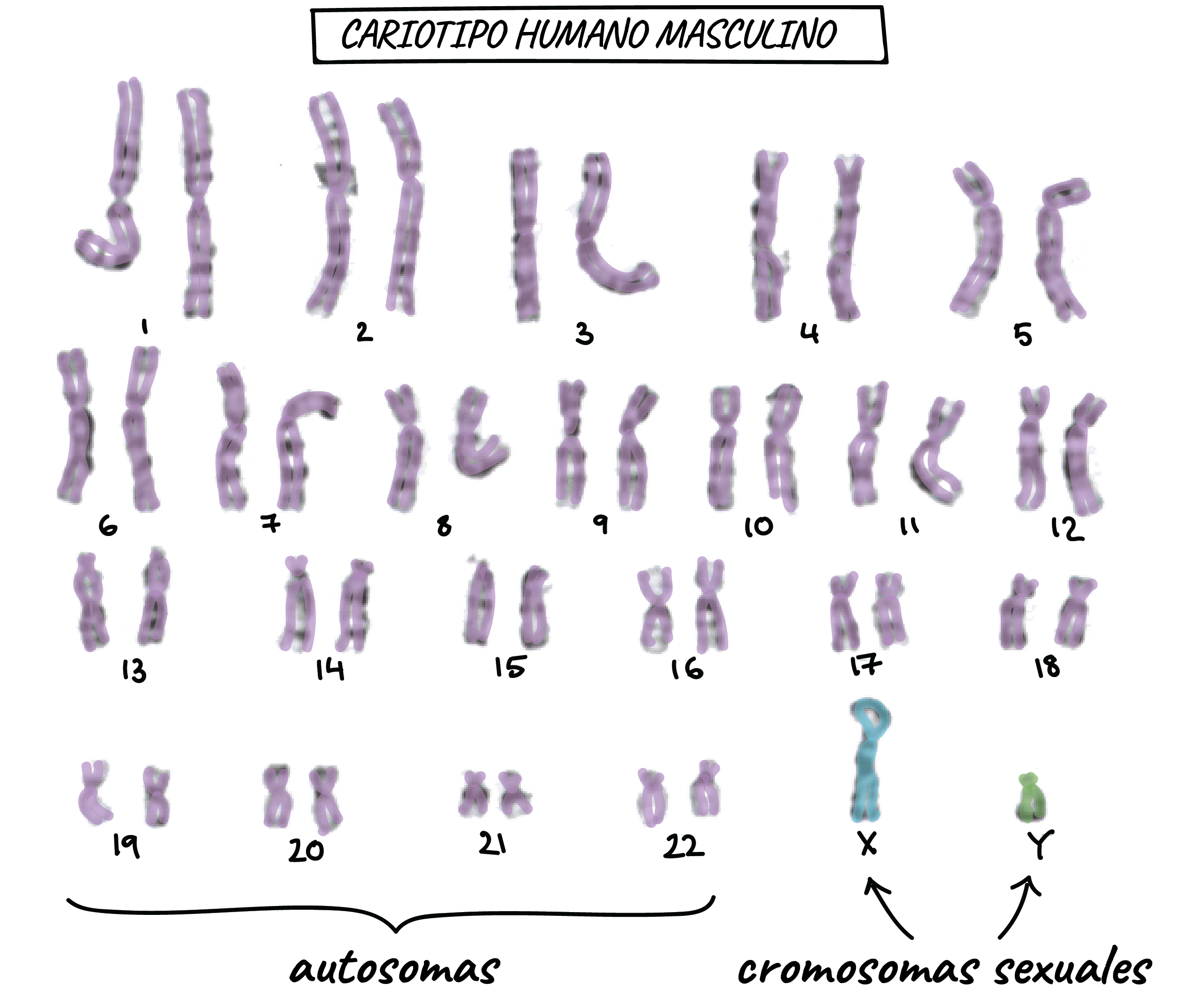La citogenética humana se centra en analizar las características de los cromosomas. Durante la división celular, conocida como mitosis, el material genético (ADN junto con proteínas) se compacta para formar estructuras llamadas cromosomas. Estos alcanzan su máxima compresión durante la etapa de metafase, lo que permite realizar el estudio citogenético sobre los cromosomas en este momento.
En la etapa de metafase, un cromosoma exhibe varios componentes distintivos:
- Dos cromátides, cada una cargando una copia del ADN.
- Un centrómero que divide el cromosoma en dos brazos, p y q, de longitud desigual en los cromosomas submetacéntricos y con un brazo p muy corto en los acrocéntricos.
- Telómeros que garantizan la estabilidad del cromosoma.
- Heterocromatina, regiones genéticas densamente empaquetadas durante la interfase.
- Eucromatina, que comprende la mayor parte del cromosoma y contiene genes activos.
- Satélites, formaciones redondeadas conectadas a las cromátides en ciertos cromosomas.
El estudio citogenético utiliza estos rasgos para analizar la constitución genética de una persona, ya que cada cromosoma tiene una morfología y tamaño consistentes. La técnica de tinción de bandas revela patrones característicos que permiten la identificación precisa de cada cromosoma y sus regiones. Por ejemplo, el locus cromosómico se describe mediante el número de par cromosómico, seguido del brazo (p o q), y el número de banda y subbanda (por ejemplo, 1q31). Las distintas técnicas de tinción generan patrones de bandas variados, siendo el más utilizado el patrón de bandas G.
alteraciones en las que estan implicadas dos o mas cromosomas
En el caso de alteraciones que involucren dos o más cromosomas, se sigue un formato específico para describirlas. Primero se menciona el cromosoma de menor número, o el cromosoma sexual si está involucrado, seguido del segundo cromosoma, separados por un punto y coma y entre paréntesis se detallan los puntos de rotura de cada cromosoma, también separados por punto y coma. En translocaciones complejas con más de dos cromosomas implicados, se menciona primero el cromosoma de menor número o el sexual, luego el cromosoma que recibe un segmento del primero, y al final el cromosoma que aporta material al primero. Por ejemplo: 46,XX,t(1;2)(p11;q21).
Cuando se trata de un cromosoma derivado de una translocación sin intercambio recíproco de material, se indica con "der" seguido de los detalles de la translocación. Por ejemplo: 46,XY,der(14)t(11;14)(q13;q32).
Las inversiones se describen con los puntos de rotura implicados, sin separar por punto y coma. Por ejemplo: 46,XY,inv(16)(p13q22).
Cuando hay material adicional cuyo origen no se conoce, se utiliza "add" seguido del cromosoma receptor y la banda afectada. Por ejemplo: 46,XY,add(14)(q32).
Los cromosomas en forma de anillo (r) y los cromosomas marcadores (mar) se mencionan al final de la fórmula. Por ejemplo: 48,XX,+r(7),+mar.
Al final de la descripción se indica el clon, especificando entre corchetes el número de metafases analizadas y el número correspondiente a cada clon, separados por barras si hay más de uno. Si hay evolución clonal, se enumeran por orden de complejidad. Si existen clones no relacionados, se indican según su tamaño, con el mayor primero, y si hay un clon normal, se menciona al final.